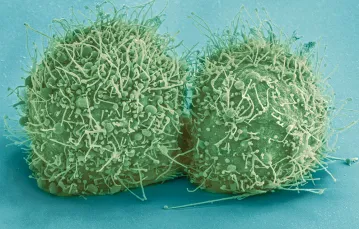
Światowa kariera Henrietty Lacks zaczęła się tuż przed jej śmiercią: te same komórki jej ciała, które spowodowały śmierć, służą do dziś badaczom tajników życia. Umierając w roku 1951 na raka szyjki macicy, na wydzielonym dla Czarnych kobiet oddziale szpitala Johns Hopkins w Baltimore, Henrietta - wnuczka niewolników - nie mogła wiedzieć, że w pewnym sensie czeka ją nieśmiertelność. I że jej śmierć ogromnie przyczyni się do powiększenia wiedzy na temat nowotworów.
Cud natury
Życie Henrietty Lacks nie obfitowało w wielkie wydarzenia. Była jednym z dziesięciorga dzieci Elizy i Johna Pleasant. Urodziła się w Wirginii, na ziemi swych przodków, niewolników, gdzie głównym sposobem utrzymania była praca na plantacji bawełny. Wyszła wcześnie za mąż za Davida Lacksa, swego ukochanego z lat młodzieńczych. Po ślubie szybko przenieśli się na przedmieścia Baltimore. David pracował w stoczni, a Henrietta rodziła mu dzieci. Mieli ich piątkę. Ostatnie przyszło na świat w listopadzie 1950 r., gdy miała zaledwie 30 lat.
Szczęście nie trwało długo. Już w trzy miesiące później Henrietta znalazła się ponownie w szpitalu. Stwierdzono raka szyjki macicy. Lekarze z Johns Hopkins Hospital w Baltimore 9 lutego 1951 r. dokonali biopsji. Pomimo szybko podjętego leczenia, Henrietta zmarła 4 października 1951 r.
Komórki pobrane w lutym dzieliły się za jej życia dokładnie przez 239 dni. I nie przestały się dzielić po jej śmierci.
Miały bowiem wyjątkowe właściwości. W przeciwieństwie do innych komórek (również nowotworowych), dzieliły się bardzo szybko i łatwo w hodowli in vitro, czyli poza organizmem. Ba, namnażały się w nowych warunkach jeszcze szybciej niż w organizmie pacjentki, dzieląc się raz na dobę. Lekarze byli tym tak zaskoczeni, że przenosili owe komórki do coraz to nowych mediów hodowlanych i obserwowali nieznane im dotąd zjawisko ciągłych podziałów. Komórki, którym nadano nazwę HeLa od pierwszych liter imienia i nazwiska dawczyni, nie robiły sobie nic ze zmian pożywek hodowlanych i mnożyły się jak oszalałe.
Dzięki komórkom HeLa odkryto m.in.:
1952 - jak hodować komórki w szkle i jak je bezpiecznie zamrażać. Umożliwiło to rozwój biotechnologii.
1953 - jak przy pomocy barwnika zwanego hematoksyliną umożliwić oglądanie chromosomów. Otworzyło to drogę m.in. do diagnozowania chorób genetycznych.
1956 - jak tworzyć komórki hybrydowe. Posłużyło to m.in. do opracowania metod mapowania genów.
1973 - jak działa salmonella.
1984 - w jaki sposób wirus HPV powoduje raka. Odkrycie niemieckiego wirusologa Haralda zur Hausena przyniosło mu Nagrodę Nobla w 2008 r. Dzięki temu odkryciu mogła powstać szczepionka.
1986 - jak przebiega mechanizm infekcji wirusem HIV.
1989 - w jaki sposób enzym zwany telomerazą zapobiega niszczeniu komórek. Przysłużyło się to badaniom nad nowotworami oraz nad długowiecznością.
1993 - jak bakterie gruźlicy atakują ludzkie komórki.
Opracowano na podstawie "Wired" 2/2010
Okazało się, że komórki HeLa są nie tylko szalone, ale i nieśmiertelne. Mają nieograniczoną zdolność do przechodzenia podziałów komórkowych właśnie dlatego, że są komórkami rakowymi. W dodatku, jako komórki raka szyjki macicy, zawierają nie tylko DNA Henrietty, ale też wirusa brodawczaka HPV 18. Jedno z białek owego wirusa powoduje, że własne białko Henrietty, o nazwie p53, było w jej komórkach bardzo szybko niszczone. A jest ono najistotniejszym obrońcą komórek przed nowotworzeniem. Stwierdzono również, że komórki HeLa mają wiele anomalii chromosomowych, wywołanych mutacją jednego z licznych genów o nazwie HLA. Ów zmieniony gen spowodował, że część chromosomu oznaczonego numerem 1 przewędrowała do chromosomu 3, a pewien fragment chromosomu 5 został kilkakrotnie powielony i też zmienił swoje miejsce na mapie chromosomowej.
To z powodu owej niezwykłej akumulacji mutacji i działania wirusa brodawczaka, komórki Henrietty utraciły cechy zwykłych komórek i uzyskały nieśmiertelność pozwalającą na namnażanie się bez końca. Nagromadzenie tych zmian odpowiada za przypadkową część cudu natury, jakim się okazały. Oczywiście mechanizm prowadzący do szalonych podziałów tych komórek opisano dopiero wiele lat po śmierci dawczyni, badając skrupulatnie ich patologie. Pozwoliło to zrozumieć przyczyny wielu typów nowotworów, jak i liczne zasady funkcjonowania zdrowych komórek.
W roku 1951 nie radzono sobie z hodowlą komórek ludzkich in vitro. Dopiero uzyskanie łatwo się dzielących komórek HeLa otworzyło przed biologami możliwości prowadzenia testów, których przedtem nie można było wykonać. Komórki te stały się niezwykle cennym materiałem badawczym. Dzięki nim można było testować działanie środków chemicznych, w tym lekarstw lub potencjalnych lekarstw, na komórki ludzkie bez szkody dla organizmu człowieka. Dzięki wprowadzeniu nowych metod biologii molekularnej, wiele lat po śmierci Henrietty Lacks można ciągle śledzić i odkrywać zmiany w genach i białkach odpowiedzialnych przed laty za wywołanie w jej organizmie raka szyjki macicy.
Zmiany, które ciągle są zagrożeniem dla milionów kobiet.
Model życia
Komórki pobrane od Henrietty Lacks trafiły do pracowni doktora George’a Geya, który od dawna próbował, choć bez większych sukcesów, hodowli komórkowej in vitro. Pierwszą osobą, która dostrzegła nadzwyczajne cechy tych komórek, była asystentka Geya, Mary Kubicek. Jej obserwacje przykuły uwagę doktora. Nie trzymał on komórek HeLa wyłącznie w swym laboratorium, lecz chętnie dzielił się nimi z innymi naukowcami.
Okazało się, że komórki te są tak żywotne i odporne na stres, że można je było przesyłać na spore odległości... zwykłą pocztą! Szybko opracowano metody ich mrożenia i bezpiecznego odmrażania. Dzięki temu można było zamrożone w ciekłym azocie lub suchym lodzie komórki przesyłać na jeszcze większe odległości. W ten sposób trafiły najpierw do laboratoriów Europy, a następnie całego świata.
Jednym z pierwszych naukowców używających z wielkim powodzeniem komórek HeLa do swych badań był pracujący nad szczepionką przeciwko polio Jonas Stalk. Można śmiało stwierdzić, że uzyskanie tej szczepionki w roku 1954 było możliwe wyłącznie dzięki użyciu komórek Henrietty.
A był to zaledwie początek ich kariery.
Dziś komórki HeLa są najczęściej używanymi komórkami w hodowli in vitro, obok komórek mysich NIH3T3 i CHO pochodzących z raka jajników chomika syryjskiego. Dzięki opracowaniu metod hodowli komórek in vitro właśnie na materiale pobranym od Henrietty, można było uzyskać setki różnych innych typów ludzkich linii komórkowych namnażających się w hodowli laboratoryjnej. Jednak żadna z nich do tej pory nie zrobiła tak zawrotnej kariery jak linia HeLa. To na nich najdogodniej prowadzić wszelkie badania wstępne. Wyniki uzyskane z analizy tych komórek sprawdza się następnie na innych liniach komórkowych. W ten sposób można się przekonać, czy dany proces albo reakcja ma charakter powszechny, czy też ograniczony wyłącznie do komórek rakowych lub jest typowa jedynie dla komórek HeLa.
Choć komórki te zachowały do dziś wiele właściwości komórek Henrietty Lacks, to jednak bardzo wiele z ich cech uległo zmianie. W trakcie milionów podziałów poza organizmem i w bardzo różnych warunkach zmieniały one liczbę chromosomów i akumulowały nowe mutacje. Dziś mają aż 82 chromosomy, czyli prawie dwa razy więcej niż normalna komórka ludzka, posiadająca ich 46. W dodatku mają one aż cztery kopie chromosomu 12 i po trzy kopie chromosomów 6, 8 i 17. Najprawdopodobniej tak zmienionym komórkom ciągle pomagają przetrwać geny wirusa brodawczaka.
Wielu naukowców uważa komórki HeLa za nadzwyczajny model ludzkiego życia.
Komórki HeLa znajdują się dziś w większości laboratoriów biologicznych i medycznych na świecie. Jest więc rzeczą zupełnie zrozumiałą, że masa wszystkich komórek uzyskanych od roku 1951 z tych kilku pierwszych przerosła wielokrotnie masę ciała dawczyni. W dodatku jej komórki, zmieniając ciągle zawartą w nich informację genetyczną, ewoluują.
Słowem, Henrietta Lacks prowadzi życie po życiu.
Etyka i pamięć
Dzięki nazwie "HeLa" wiemy dziś, od kogo pochodziły owe komórki. To dość rzadka sytuacja w nauce, a chyba jedyna w przypadku tak rozpowszechnionego materiału badawczego. Obecnie, z powodów etycznych, jest nie do pomyślenia, by komórkom ludzkim nadawać nazwy głoszące wszem i wobec historię ich dawcy. Jednak w latach 50. XX wieku dzisiejsze standardy etyczne nie obowiązywały. Trudno więc mieć za złe doktorowi Geyowi, że przekazał potomnym poufne informacje dotyczące Henrietty.
Rodzina zmarłej nie wiedziała o istnieniu komórek HeLa aż do wczesnych lat 70. XX wieku. Dwadzieścia lat po śmierci dawczyni próby uzyskania gratyfikacji okazały się nieskuteczne. Ani Henrietta, ani jej dzieci nie miały więc żadnych bezpośrednich korzyści z udostępnienia nauce komórek. Jednak korzyści pośrednie, i to dla całej ludzkości, są tak wielkie, że pamięć o Henrietcie Lacks jest ciągle żywa. W lutym każdego roku w Turner Station w Wirginii, gdzie mieszkali państwo Lacks, obchodzony jest Henrietta Lacks Day. Kongres Stanów Zjednoczonych ogłosił rezolucję przygotowaną przez republikańskiego senatora Roberta Ehrlicha, upamiętniającą panią Lacks. Charlene Gilbert, również czarnoskóra, nakręciła o niej film zatytułowany "Colored Bodies: Henrietta Lacks and the HeLa cells" (colored bodies, czyli "kolorowe ciała" to dosłowne tłumaczenie słowa "chromosom": chromo - kolor, soma - ciało). Kilka dni temu ukazała się książka pt. "The Immortal Life of Henrietta Lacks" ("Nieśmiertelne życie Henrietty Lacks").
Komórki Henrietty żyją dalej po jej śmierci, trochę tak, jak dzieło przedłuża życie artysty. Różnica jest jednak wielkiego kalibru: HeLa to nie dzieło, lecz część jej ciała. W dodatku ta, która ją zabiła. Niezwykłym symbolem jest fakt, że tak przydatne dla nauki komórki pochodzą od córki czarnych niewolników, którzy doznali tyle zła od białych. Dzisiaj jej komórki dają nadzieję na ratowanie życia wszystkim, bez względu na kolor skóry.
Dr hab. JACEK KUBIAK jest biologiem, pracuje w Narodowym Centrum Badań Naukowych (CNRS) w Rennes we Francji. Stale współpracuje z "TP".
„Tygodnik Powszechny” – jedyny polski tygodnik społeczno-kulturalny.
30 tys. Czytelniczek i Czytelników. Najlepsze Autorki i najlepsi Autorzy.
Wspólnota, która myśli samodzielnie.