Wykupienie dostępu pozwoli Ci czytać artykuły wysokiej jakości i wspierać niezależne dziennikarstwo w wymagających dla wydawców czasach. Rośnij z nami! Pełna oferta →
Dwa lata temu 84-letni Douglas Waters z Croydon w południowym Londynie nie był w stanie przeczytać nawet bardzo dużych liter przez szkło powiększające. Dziś, dzięki eksperymentalnej terapii AMD, w zwyczajnych okularach czyta gazetę.
Choroba
Światło dostające się do oka przez źrenicę pada na siatkówkę, którą tworzy wiele warstw wyspecjalizowanych komórek wyściełających wnętrze oka. W światłoczułej warstwie pręcików i czopków światło jest absorbowane i generowane są impulsy elektryczne, przekazywane przez nerw wzrokowy do ośrodków korowych w tylnej części mózgu, które z morza sygnałów krok po kroku konstruują to, co widzimy. Pod warstwą fotoreceptorów znajduje się tzw. nabłonek barwnikowy siatkówki, oddzielony błoną Brucha od naczyniówki – systemu naczyń i komór wypełnionych krwią, która odżywia komórki siatkówki.
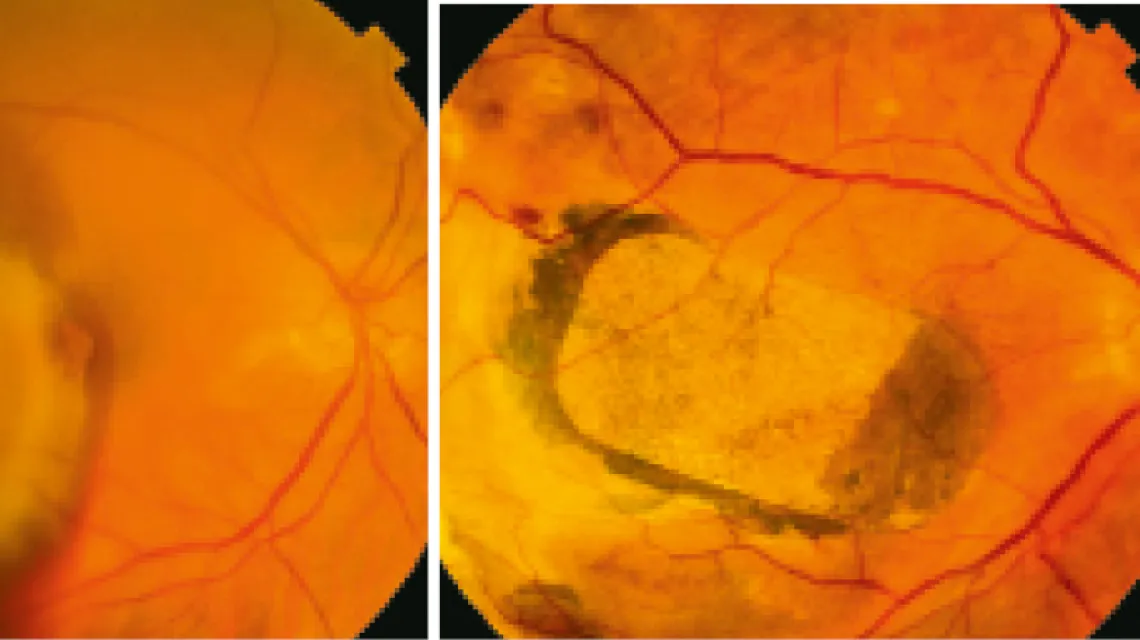
Zwyrodnienie plamki żółtej związane z wiekiem (ang. Age-related Macular Degeneration, AMD) jest poważną chorobą oczu, dotykającą ok. 5 proc. populacji powyżej 60. roku życia. Przewiduje się, że do 2020 r. na AMD zachoruje 196 mln ludzi na świecie – już teraz jest to najczęstsza przyczyna utraty wzroku wśród osób po pięćdziesiątce w krajach rozwiniętych. Ściśle rzecz biorąc, choroba ta zwykle nie prowadzi do całkowitej ślepoty, ale upośledza obszar plamki żółtej – rejon siatkówki, gdzie znajduje się największe zagęszczenie fotoreceptorów, umożliwiające najlepszą rozdzielczość widzenia. To ten obszar wykorzystujemy, gdy na czymś skupiamy wzrok, czytamy albo rozpoznajemy czyjąś twarz.
Bezradność
Nie są znane ani przyczyny zwyrodnienia (nie wiadomo np., dlaczego dotyka ono jedynie obszar plamki żółtej), ani skuteczne metody jego leczenia. W odmianie „mokrej”, w której dochodzi do niekontrolowanego wzrostu naczyń krwionośnych, pewne efekty lecznicze daje regularne podawanie leków do gałki ocznej. Przy 6 mln zastrzyków rocznie w skali świata staje się to wyzwaniem dla służby zdrowia, nawet w bogatych krajach. W przypadku odmiany „suchej” degeneracji ulegają kluczowe warstwy siatkówki: nabłonek barwnikowy, fotoreceptory i naczynia włosowate. Ta odmiana AMD stanowi zdecydowaną większość przypadków i nie są w tej chwili dostępne żadne strategie jej leczenia.
CZYTAJ TAKŻE:
W ciągu ostatnich kilkunastu lat próbowano różnymi sposobami przywrócić widzenie w obszarze plamki żółtej u pacjentów z AMD, m.in. przy pomocy trudnych zabiegów, w których odkleja się siatkówkę i obraca ją tak, by w obszarze plamki znalazły się zdrowe komórki, albo wykonując przeszczepy komórek z innych, peryferyjnych obszarów siatkówki. Niektóre z tych zabiegów dały obiecujące rezultaty, ale ze względu na złożoność procedury żaden z nich nie daje nadziei na zastosowanie w skali dziesiątek czy setek tysięcy pacjentów.
Ich szansą mogą być aktualnie będące w eksperymentalnej fazie terapie wykorzystujące tzw. komórki macierzyste.
Nadzieja
Komórki macierzyste mają unikalne właściwości, pozwalające im różnicować się w wyspecjalizowane komórki organizmu. Mogą być źródłem prawie dowolnych komórek – mięśni, nerwów czy komórek wątroby – jeśli tylko potrafimy odpowiednio ukierunkować ich rozwój. Zarodki składają się m.in. właśnie z takich komórek. Odpowiednio pokierowane, w procesach, o których ciągle niewiele wiemy, przekształcają się one w poszczególne tkanki i narządy. W mniejszych ilościach komórki macierzyste występują także w dorosłym organizmie, jednak z reguły nie są aż tak plastyczne (nie są to tzw. pluripotencjalne komórki macierzyste).
W ciągu ostatnich kilku dekad naukowcy opanowali metody hodowli różnych komórek na bazie komórek macierzystych pochodzących zarówno z zarodków, jak i pobranych od dorosłych osobników. Te ostatnie – ze względu na kontrowersje etyczne wokół wykorzystywania zarodków – próbuje się tak przeprogramowywać, by stały się równie plastyczne, jak (pluripotencjalne) komórki zarodkowe.
Obecnie kilka grup badawczych na świecie prowadzi zaawansowane eksperymenty, w tym w fazie klinicznej, z udziałem pacjentów, w których przy pomocy komórek macierzystych próbuje się odbudować zdegenerowane w wyniku AMD warstwy siatkówki.
Wyniki
Jedna z takich grup, kierowana przez prof. Petera Coffeya i prof. Lyndona Da Cruza, opublikowała w marcu tego roku w czasopiśmie „Nature Biotechnology” wyniki pierwszej próby klinicznej, przeprowadzonej na dwójce pacjentów w Moorfields Eye Hospital w Londynie – jednym z nich był wspomniany Douglas Waters. Na bazie linii komórkowej SHEF-1 (nazwa pochodzi od University of Sheffield) na podłożu z cieniutkiej perforowanej folii z plastiku (takiego samego, z którego wytwarzane są butelki do napojów) wyhodowano warstwę komórek nabłonka barwnikowego siatkówki. Tak przygotowaną łatę o wymiarach 3 na 6 mm wprowadzono między warstwy siatkówki podczas operacji trwającej niecałe dwie godziny. Z początku dwa eksperymentalne zabiegi miały na celu przede wszystkim stwierdzenie, czy terapia taka jest bezpieczna, jednak ich wyniki przerosły najśmielsze oczekiwania lekarzy, biologów i inżynierów zaangażowanych w rozpoczęty ponad dziesięć lat temu „London Project to Cure Blindness”. Po roku od zabiegu pacjenci, którzy wcześniej z trudem rozpoznawali przedmioty wielkości książki, byli w stanie czytać z prędkością 50 i 80 słów na minutę.
Choć do pierwszych operacji wybrano pacjentów z mokrą formą AMD, nie widać fundamentalnych powodów, dla których terapia z użyciem pokrytego komórkami nabłonka implantu nie mogłaby działać w przypadku formy suchej. W najbliższych miesiącach naukowcy z Londynu zamierzają przeprowadzić kolejne zabiegi. Jeśli ich prognozy się sprawdzą, za około pięć lat terapia powinna być dopuszczona do powszechnego stosowania i ma szansę stać się rutynowym, tanim zabiegiem, jak dziś leczenie zaćmy przez wstawienie polimerowej soczewki. ©
Prawo:
W WIELKIEJ BRYTANII użycie ludzkich zarodkowych komórek macierzystych jest uregulowane szczegółowymi przepisami i ograniczone do kilku obszarów: badań nad leczeniem niepłodności, badań nad przyczynami chorób wrodzonych, badań nad przyczynami poronień, badań nad rozwojem nowych, bardziej skutecznych metod antykoncepcji, badań nad uszkodzeniami genów i chromosomów, badań nad rozwojem zarodków oraz badań nad przyczynami i sposobami leczenia poważnych chorób. Obecnie UK Stem Cell Bank przechowuje 23 linie ludzkich komórek macierzystych, zdeponowanych przez grupy badawcze z kilku brytyjskich uniwersytetów i firmę Pfizer, i udostępnia je do badań po spełnieniu rygorystycznych wymagań.
W POLSCE nie ma szczegółowych przepisów regulujących użycie ludzkich zarodkowych komórek macierzystych.